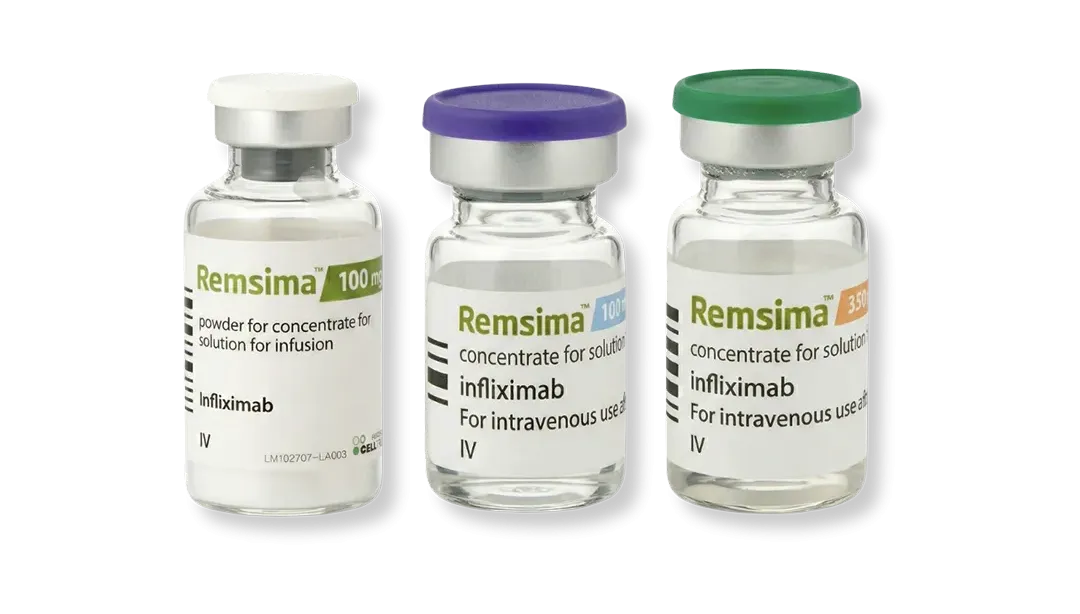
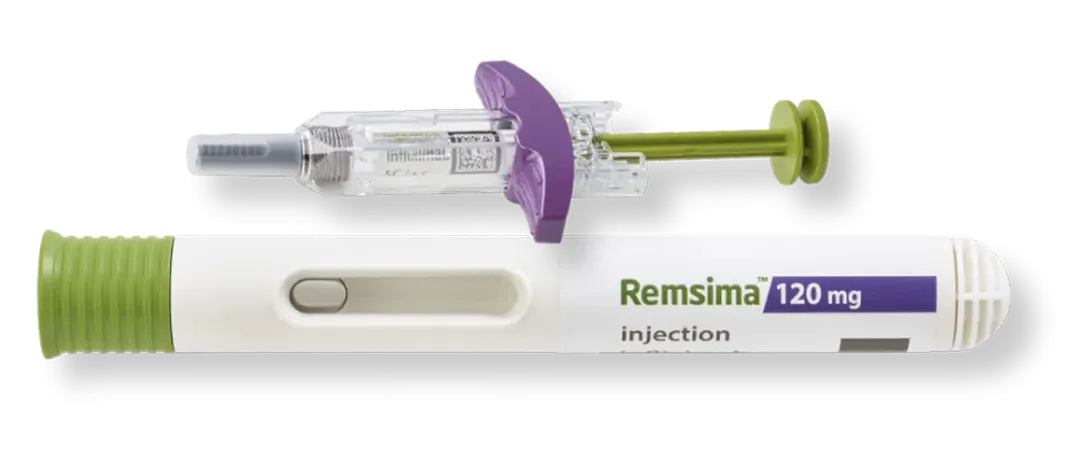
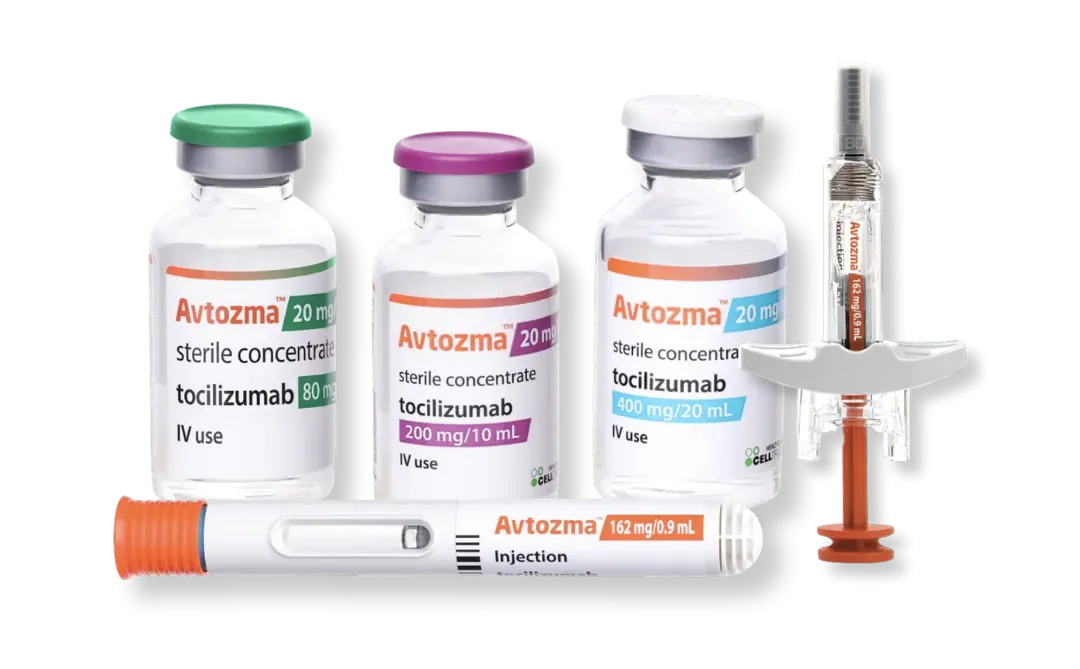
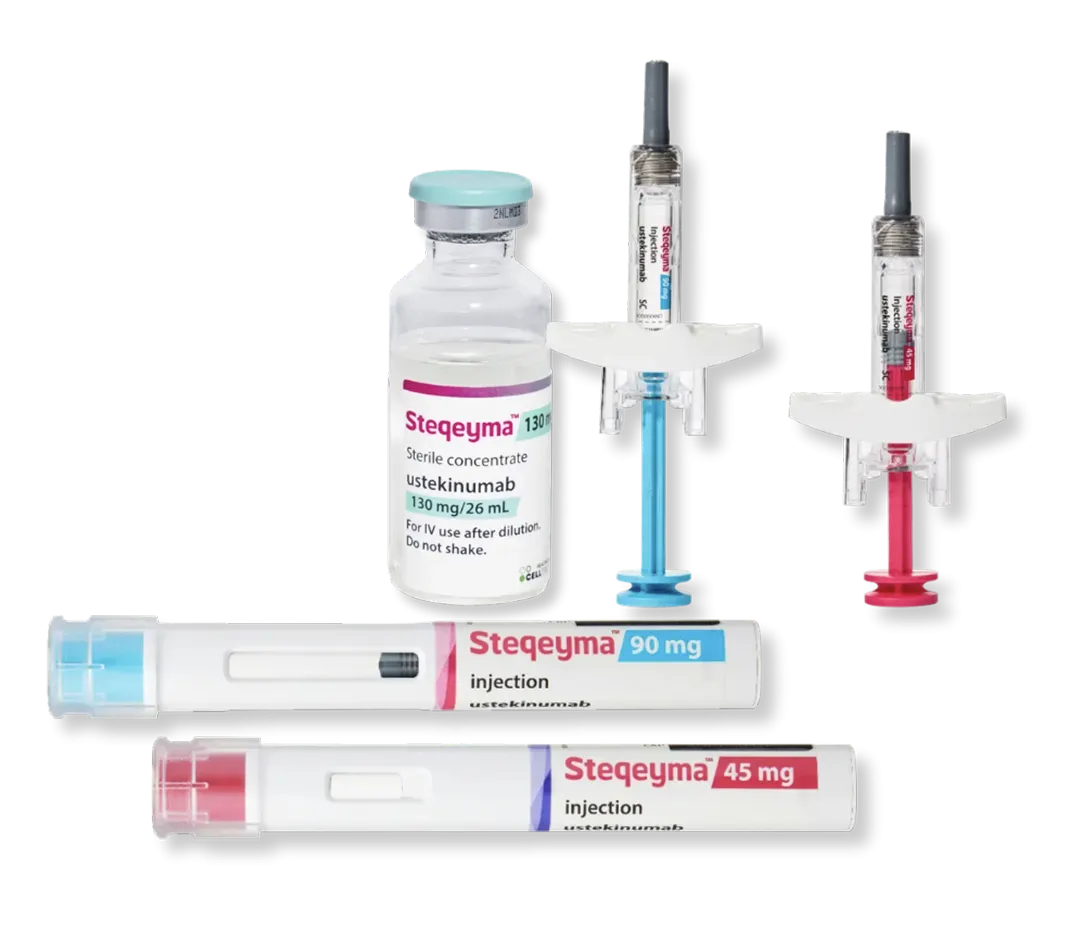
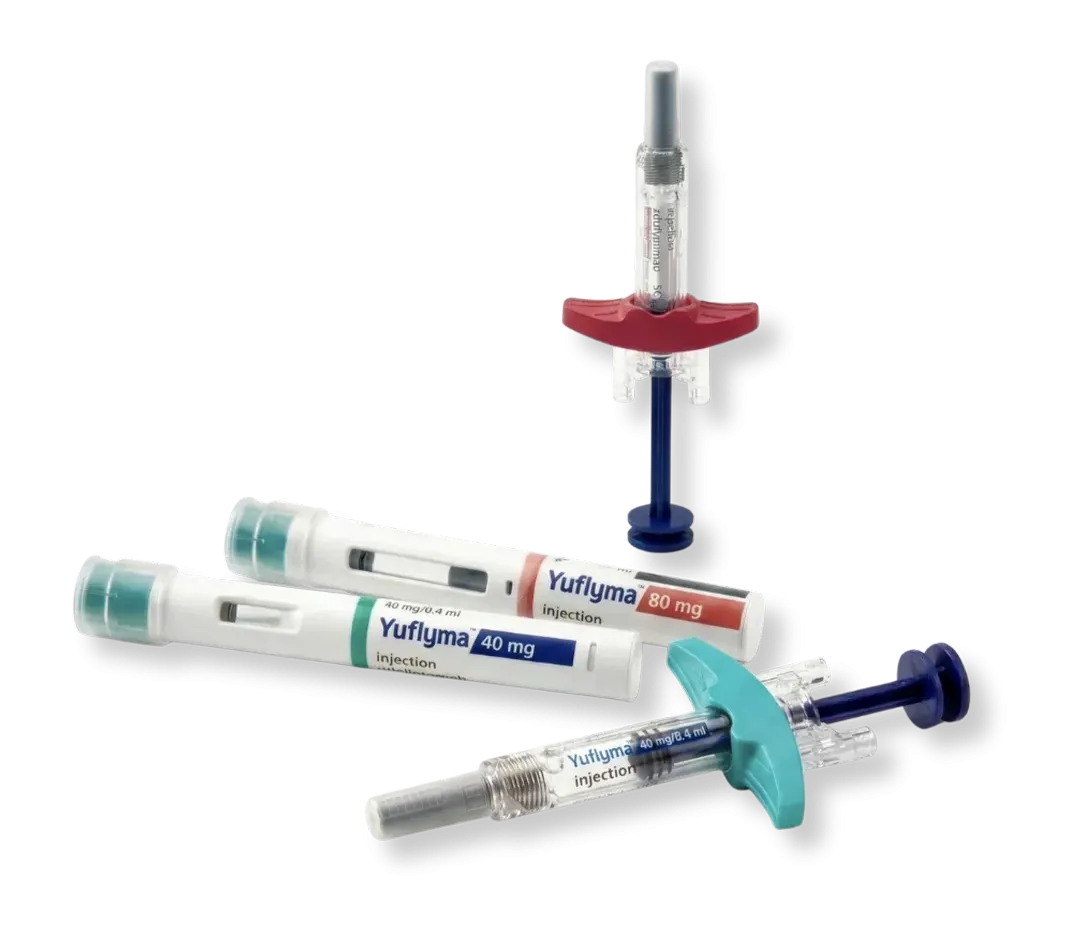
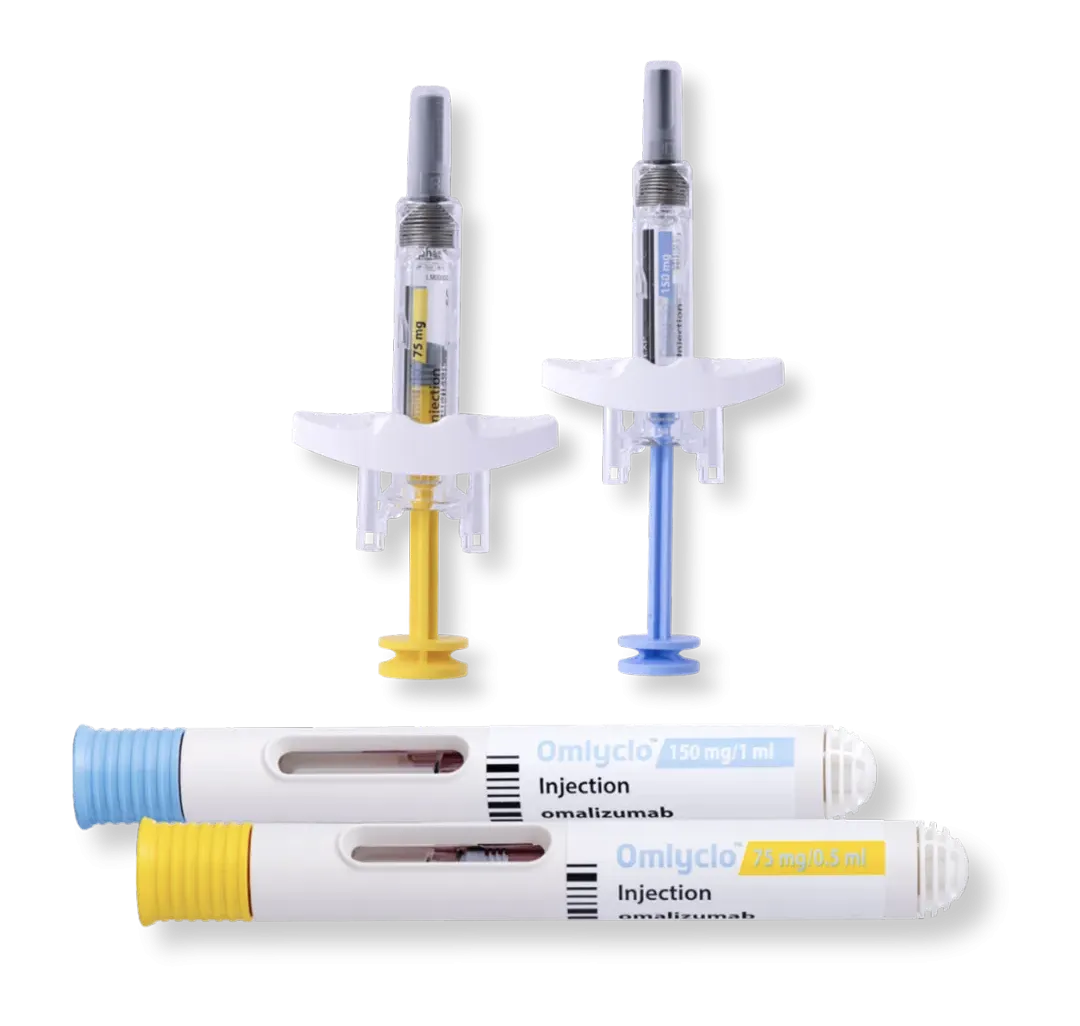
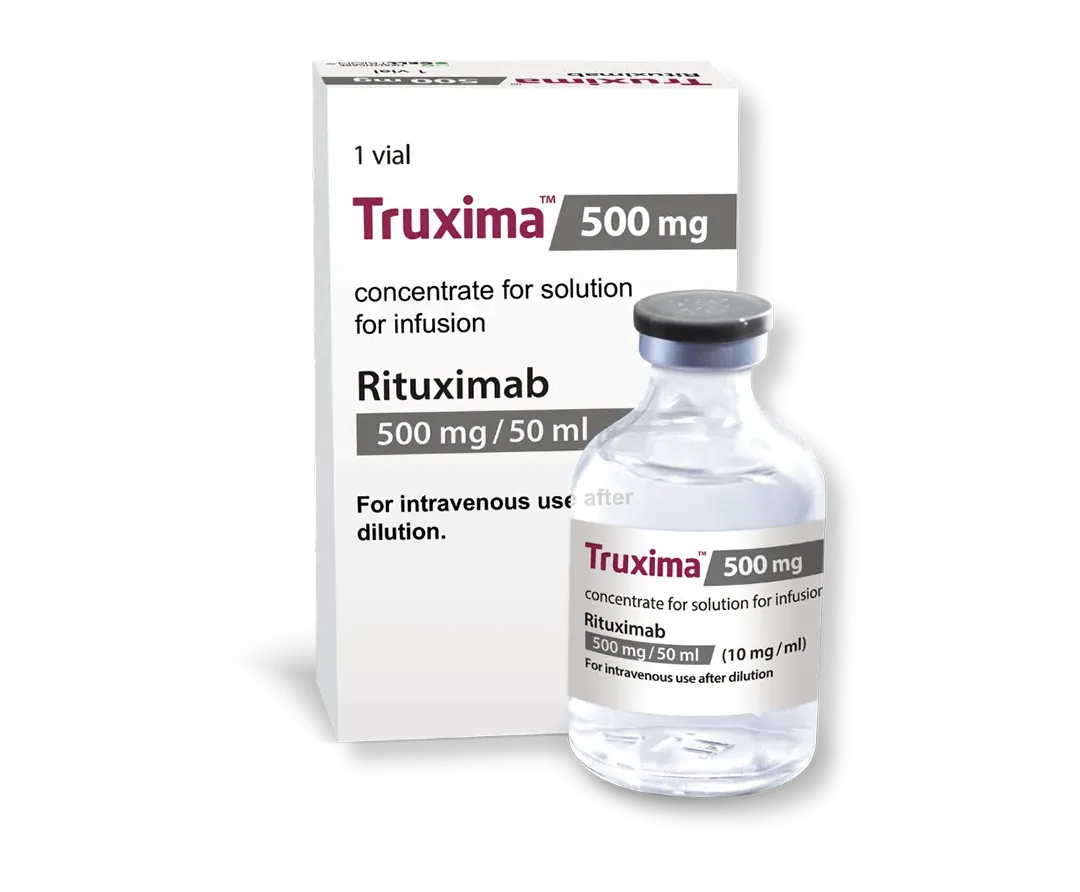
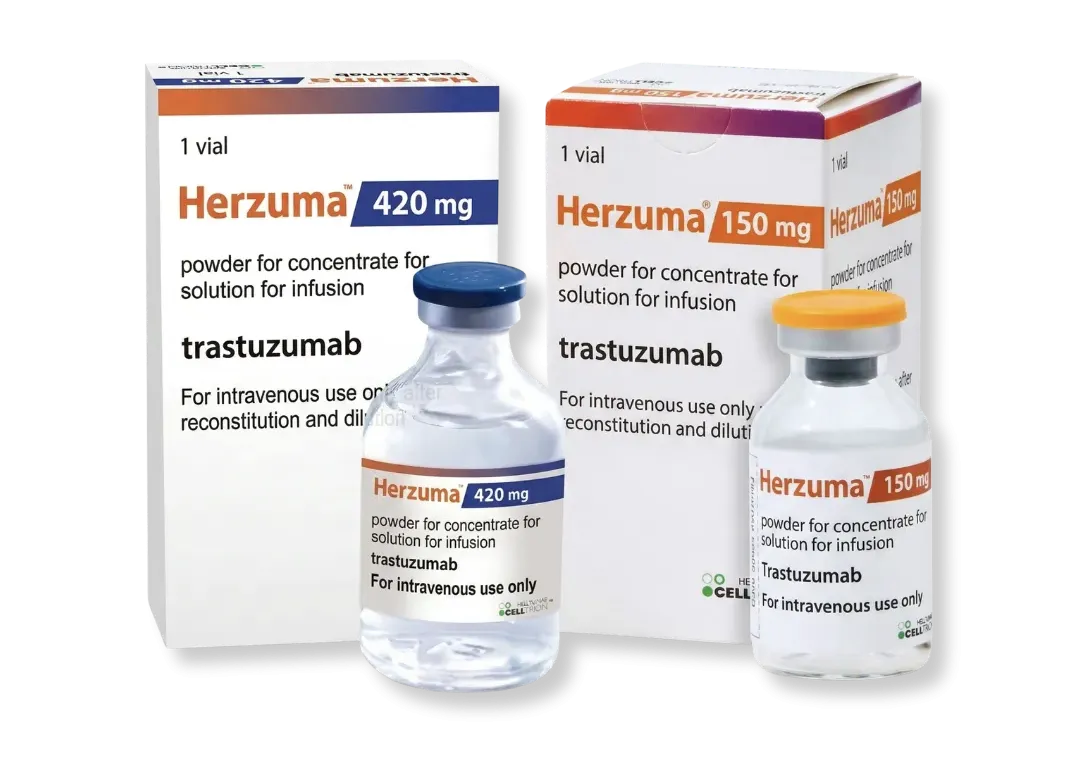
First Mover and Now Europe’s Largest mAb Biosimilar Portfolio1
Our 12 EMA Approved Products For Hospital Pharmacists
Built on Trust, Toward Innovation.
Some of the products might not be marketed in your country. Check with your health authorities the availability of the products in your country.
ES–26-00003 Febrero 2026